
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Периодическая система элементов Д.И. Менделеева

Таблица 10
Мантиссы логарифмов

Таблица 10 продолжение
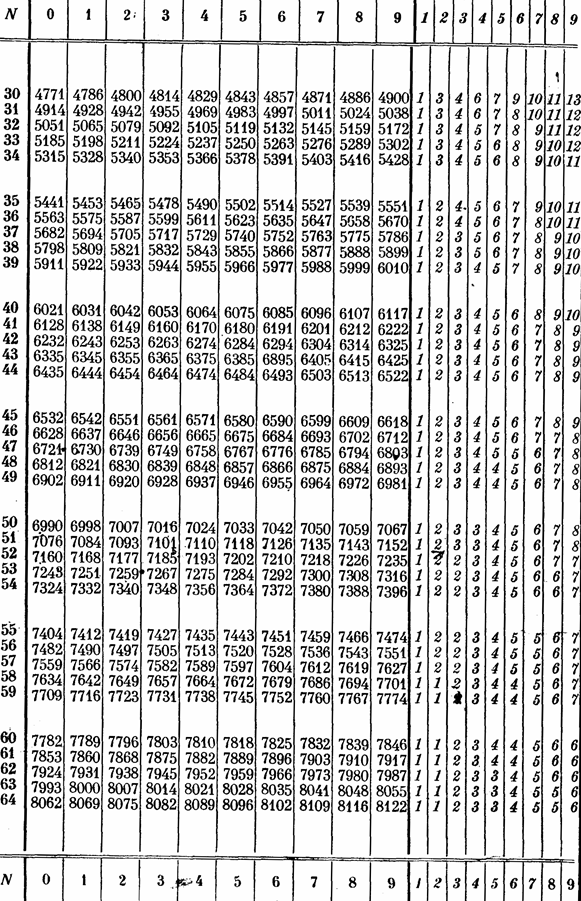
Таблица 10 продолжение
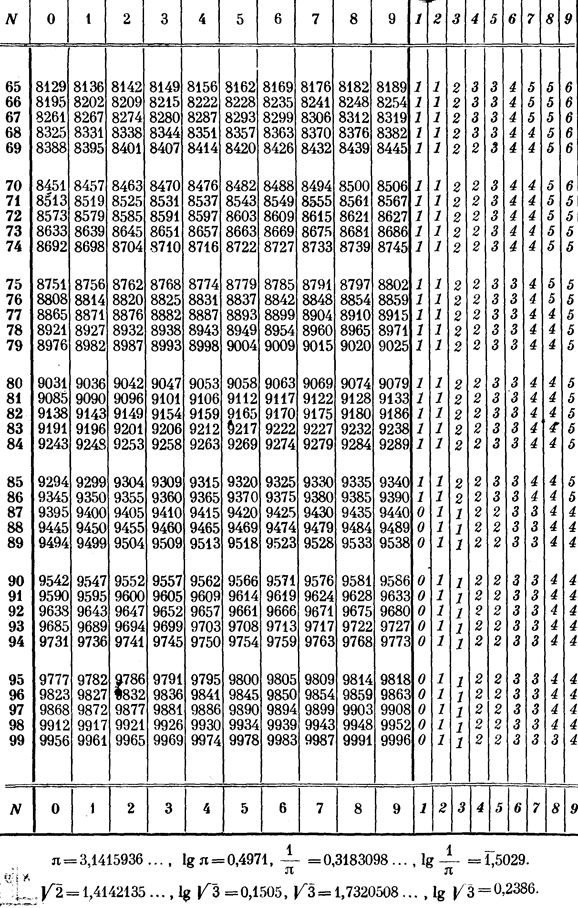
ОГЛАВЛЕНИЕ
Введение......................................................... 3
Раздел 1. Теоретические основы общей химии......................... 4
Глава 1. Основные понятия и законы химии ...................... 4
Глава 2. Основные классы неорганических соединений ............. 6
Глава 3. Строение атома. Периодический закон Д.И.Менделеева.
Периодическая система химических элементов..... ....... 11
Глава 4. Химическая связь. Строение вещества........ .......... 24
Глава 5. Химическая термодинамика.. ......................... 34
Глава 6. Кинетика химических реакций. Химическое равновесие ... 42
Глава 7. Химия растворов ..................................... 52
Глава 8. Комплексные соединения .............................. 65
Глава 9. Окислительно-восстановительные реакции .............. 72Раздел 2. Решение расчётных задач ................................. 81
Глава 1. Расчёт концентраций растворов........................ 81
Глава 2. Вычисления в титриметрическом (объёмном) анализе...... 85
Глава 3. Вычисление водородного показателя.................... 88
Раздел 3. Контрольные задания.....................................91
3.1. Варианты контрольных заданий........................... 92
3.2. Контрольные задания по курсу «Общая химия»............... 95
3.3. Контрольные задания «Решение расчётных задач»............ 107
Словарь химических терминов..................................... 111
Рекомендуемая литература........................................ 115
Приложение.................................................... 116
Таблица 1.
Названия кислот, солей и кислотных остатков.................. 116
Таблица 2.
Термодинамические константы некоторых веществ.............. 117
Таблица 3.
Степень диссоциации кислот, оснований и солей в 0,1н. водных
растворах (при 18оС)........................................ 121
Таблица 4.
Растворимость солей, кислот и оснований в воде................. 122
Таблица 5.
Константы диссоциации кислот............................... 123
Таблица 6.
Константы нестойкости комплексных ионов..................... 123
Таблица 7.
Плотности растворов кислот, щелочей, аммиака различной
концентрации (при 15оС)..................................... 124
Таблица 8.
Плотности растворов солей различной концентрации............. 125
Таблица 9.
Периодическая система элементов Д.И.Менделеева............... 126
Таблица 10.
Мантиссы логарифмов........................................ 127
· Если у элемента есть латинское название, то используется оно.
[*] ПСЭ – периодическая система элементов Д.И.Менделеева.
[†] Термодинамические константы некоторых веществ приведены в табл.2 (Приложение).
* Значения плотностей растворов кислот, щелочей и солей различной концентрации приведены в табл.7 и 8 (Приложение).
[‡] Значения констант диссоциации приведены в табл.5 (Приложение)
[§] Значения степеней диссоциации для некоторых электролитов приведены в табл.3 (Приложение).
[**] Примеры решения задач по расчетам концентраций растворов и водородного показателя приводятся в разделе 2 «Решение задач».
* Данный раздел относится к дисциплине «Решение задач по химии». Усвоение этого материала необходимо для обработки результатов титриметрического анализа в курсе «Аналитическая химия», а также при изучении дисциплины «Физическая и коллоидная химия».
* Указать: металл или неметалл, возбуждённые состояния, валентные электроны, представить формулы химических соединений при минимальной и максимальной валентностях, назвать их.
* Термодинамические величины см. Табл.2 Приложения.
* Значения плотности растворов см. табл.7,8 (Приложение).
* Сокращения: к –кристаллический; ж – жидкий; г – газообразный; ам – аморфный.
* 1. Для сильных электролитов приведенные цифры представляют собой кажущиеся степени диссоциации, определённые по электропроводности растворов.
2. Цифры для двух- и многоосновных кислот относятся к первой ступени их диссоциации.
* Р – растворимое вещество; М – малорастворимое; Н – нерастворимое. Прочерк означает, что вещество не существует в растворе или разлагается водой;? – нет достоверных сведений о существовании соединения.
Не нашли, что искали? Воспользуйтесь поиском: