
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Колориметрический метод определения нитритов
Приборы и посуда: ФЭК, пипетки на 1 и 5 мл, колбы на 100 мл, мерные цилиндры на 100 мл, пробирки.
Реактивы:
1)реактив Грисса;
2)стандартный раствор азотистокислого натрия, в 1 мл которого содержится 0,001 мг азота нитритов.
Приготовление реактива Грисса; 0,2 г альфа-нафталамина растворяют в 20 мл дистиллированной воды при нагревании в фарфоровой чашке и смешивают в другой посуде со 150 мл 12%-й уксусной кислоты. При переливании содержимого чашки фиолетовые капли нерастворившегося вещества остаются на дне. Одновременно растворяют 0,5 г сульфаниловой кислоты в 150 мл 12%-й уксусной кислоты. Оба раствора сливают вместе и хранят в темной склянке с притертой крышкой (реактив должен быть бесцветным).
Приготовление стандартного раствора: для этого отвешивают 4,927 г азотнокислого натрия и растворяют в 1 л дистиллированной воды; к 1 мл этого основного раствора в мерной колбе добавляют до 1000 мл дистиллированной воды и получают рабочий раствор, в 1 мл которого содержится 0,001 мг азота нитритов.
Методика исследования. В одну колбу наливают 100 мл рабочего стандартного раствора, а в другую — 100 мл исследуемой воды; в обе колбы добавляют по 5 мл реактива Грисса. Колбы с раствором помещают в водяную баню при температуре 50-60 0С на 10 мин. При содержании в воде азота нитритов более 0,3 мг/л после добавления реактива вода окрашивается в желтый цвет. В таких случаях добавляют дистиллированную воду до розового окрашивания и при окончательном расчете полученную величину умножают на степень разведения. После этого стандартный раствор нитритов натрия и исследуемую воду колориметрируют на ФЭК при зеленом светофильтре (№ 6) в кюветах 1-5 см. Расчеты ведут по формуле:
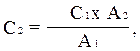
где С2 — концентрация нитратного азота в исследуемой воде, мг/л; Сх — концентрация нитритного азота в стандартном растворе нитрита калия, мг/л; А1 — оптическая плотность стандартного раствора нитрита натрия; А2 — оптическая плотность исследуемой воды.
Приближенный метод определения нитритов. В пробирку наливают 10 мл воды и добавляют 0,5 мл реактива Грисса, содержимое пробирки в течение 4 мин нагревают до температуры 70-80°С (при комнатной температуре раствор исследуют через 20 мин после добавления реактива) и сравнивают с данными таблицы 39.
Азот нитратов. Принцип исследования заключается в том, что азотнокислые соли переводятся раствором фенола в серной кислоте в пикриновую кислоту, последняя после добавления аммиака образует пикрат аммония желтого цвета.
Таблица 39
Не нашли, что искали? Воспользуйтесь поиском: