
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Алтыншы аналитикалық топ катиондары
Алтыншы аналитикалық топқа мына катиондар жатады: Cu2+, Hg2+, Co2+, Ni2+, Cd2+.
Бұл топтың хлоридтері, сульфаттары және нитраттары суда жақсы ериді. Мыс (II) тұздарының ерітінділері көгілдір түске, кобальт (II) тұздарының ерітінділері – ашық-қызыл түске, ал никель (II) тұздарының ерітінділері – жасыл түске боялған.
Бұл топ катиондарының гидроксидтері нашар еритін әлсіз электролиттер болып саналады. Cu(OH)2, Hg(OH)2 гидроксидтері - тұрақсыз, олар өздеріне сәйкес оксидке және суға ыдырайды. Мыс гидроксиді қыздырғанда ыдырайды, ал сынап гидроксиді қалыпты температурада ыдырайды.

Бұл алтыншы аналитикалық топ катиондарына комплекс түзу реакциялары тән. Топтық реагенті - аммиак ерітіндіс(NH4OH).
Тәжірибе. 5 пробиркаға 3 тамшыдан мыстың (II), сынаптың (II), кадмийдің (II), никелдің (II) және кобальттың (II) ерітінділерін құйып, оған 25%- тік аммоний ерітіндісінен 3 тамшы тамызып, шыны таяқшамен араластырыңдар. Түскен тұнбаның түсіне көңіл бөліңдер. Содан кейін әр пробиркаға 6 тамшы концентрлі аммиак ерітіндісін (NH4OH) қосып, тағы да шыны таяқшамен араластырыңдар. Сонымен қатар Hg2+, Co2+ катиондары бар ерітінділерге аммоний хлоридінің NH4Cl бірнеше кристалдарын қосыңдар:
CuSO4 + 4NH4OH =  + 4H2O
+ 4H2O
Cu2+ + 4NH4OH =  + 4H2O
+ 4H2O
HgCl2 + 4NH4OH = 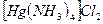 + 4H2O
+ 4H2O
Hg2+ + 4NH4OH =  + 4H2O
+ 4H2O
CdCl2 + 4NH4OH = 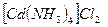 + 4H2O
+ 4H2O
Cd2+ + 4NH4OH =  + 4H2O
+ 4H2O
NiCl2 + 6NH4OH =  + 6H2O
+ 6H2O
Ni2+ + 6NH4OH = 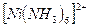 + 6H2O
+ 6H2O
CoCl2 + 6NH4OH =  + 6H2O
+ 6H2O
Co2+ + 6NH4OH =  + 6H2O
+ 6H2O
Мыс катионының Cu2+ дербес реакциялары
І. Күйдіргіш сілтілер мыс (II) тұзының ерітіндісімен көгілдір түсті мыс (II) гидроксидін түзеді:
CuSO4 + 2KOH = Cu(OH)2 ↓ + K2SO4
Cu2+ + 2OH- = Cu(OH)2 ↓
Тұнба концентрлі аммиак ерітіндісінде ериді.
1-тәжірибе. 2 тамшы мыс (II) тұзының ерітіндісіне 2 тамшы сілті NaOH ерітіндісін қосып, тұнбаның түзілуіне назар аударыңдар.
II. Калий гексацианоферраты (II) 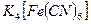 мыс (II) тұзының әлсізқышқылдық немесе бейтарап ерітіндісімен әрекеттесіп, қызыл-сұр түсті мыс гексацианоферратын (II) түзеді:
мыс (II) тұзының әлсізқышқылдық немесе бейтарап ерітіндісімен әрекеттесіп, қызыл-сұр түсті мыс гексацианоферратын (II) түзеді:
2CuSO4 + 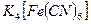 =
=  ↓ + 2K2SO4
↓ + 2K2SO4
2Cu2+ +  =
=  ↓
↓
Тұнба сұйытылған қышқылдарда ерімейді, ал аммиакта ериді.
2-тәжірибе. 2 тамшы мыс тұзының ерітіндісіне 2 тамшы калий гексацианоферратын (II) қосып, түзілген тұнбаға көңіл аударыңдар.
Сынап катионының Hg2+ дербес реакциялары
HgHРПр
I. Күйдіргіш сілтілер сынап (II) тұзының ерітіндісімен қара түсті сынап оксиді HgO тұнбасын береді:
Hg(NO3)2 + 2KOH = HgO↓ + H2O + 2KNO3
Hg2+ + 2OH- + HgO↓ + H2O
Тұнба қышқылдарда оңай ериді.
1-тәжірибе. 2 тамшы сынап (II) тұзының ерітіндісіне 2 тамшы сілті NaOH ерітіндісін қосыңдар.
II. Калий иодиді KJ сынап (II) тұзымен қызыл түсті сынап (II) иодидінің HgJ2 тұнбасын береді:
Hg(NO3)2 + 2KJ = HgJ2↓ + 2KNO3
Hg2+ + 2J- = HgJ2↓
Тұнба реактивтің артық мөлшерінде түссіз комплексті қосылыс түзеді:
HgJ2↓ + 2KJ = 
2-тәжірибе. Пробиркаға 2 тамшы сынап (II) нитраты Hg(NO3)2 ерітіндісін құйып, оған алдымен калий иодиді ерітіндісінен 2 тамшы, содан кейін артық мөлшерін қосыңдар. Тұнбаның түзілуіне және оның еруіне назар аударыңдар.
Кадмий катионының Cd2+ дербес реакциялары
І. Күйдіргіш сілтілер кадмий тұзының ерітіндісімен ақ түсті кадмий (II) гидроксидін түзеді:
CdCl2 + 2NaOH = Cd(OH)2 ↓ + 2NaCl
Cd2+ + 2OH- = Cd(OH)2 ↓
1-тәжірибе. 2-3 тамшы кадмий тұзының ерітіндісіне 1-2 тамшы сілті NaOH ерітіндісін қосыңдар. Тұнбаның түзілуіне және оның түсіне назар аударыңдар.
Кобальт Сo2+ катионының дербес реакциялары
Кобальт катионы сулы ерітінділерде қызғылт-күлгін түсті (розово-фиолетовый) береді.
І. Аммоний (NH4SCN) немесе калий роданиді (KSCN) кобальт катионымен Сo2+ комплексті тұз түзеді:
CoCl2 + 4NH4SCN ↔  + 2NH4Cl
+ 2NH4Cl
Co2+ + 4SCN- ↔ 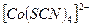
Аммоний тетрароданокобальтаты (II)  әдемі көкшіл түсті береді; ал
әдемі көкшіл түсті береді; ал 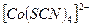 ионы - тұрақсыз және сулы ерітінділерде тез ыдырап кетеді. Егер ерітіндіге изоамил спиртін қосып, қатты шайқасақ, онда бұл комплекс еріткішке ауысып, спирт қабатын көк түске бояйды.
ионы - тұрақсыз және сулы ерітінділерде тез ыдырап кетеді. Егер ерітіндіге изоамил спиртін қосып, қатты шайқасақ, онда бұл комплекс еріткішке ауысып, спирт қабатын көк түске бояйды.
1-тәжірибе. Пробиркаға 2-3 тамшы кобальт (II) тұзының ерітіндісін құйып, оған 8-10 тамшы қаныққан аммоний роданиді ерітіндісін және 5-6 тамшы изоамил спиртін қосып, қатты шайқаңдар. Егер кобальт катионы бар болса, онда беткі қабат ашық-көк түске боялады.
IІ. Күйдіргіш сілтілер кобальт тұзының ерітіндісімен кобальттың (II) негіздік тұзын түзеді:
CoCl2 + NaOH = CoOHCl ↓ + NaCl
Co2+ +Cl- + OH- = CoOHCl ↓ +
CoOHCl ↓ + NaOH = Cо(OH)2 ↓ + NaCl
2-тәжірибе. 3-4 тамшы кобальт тұзының ерітіндісіне 1-2 тамшы сілті NaOH ерітіндісін қосыңдар. Қоспаны әбден араластырыңдар. Тұнбаның түсіне назар аударыңдар. Сосын осы түскен тұнбаға тағы да 2-3 тамшы NaOH ерітіндісін қосындар. Тұнбаның түсі өзгере ме? Жүрген процесті түсіндіріңдер және реакция теңдеуін жазыңдар.
Никель катионының Ni2+ дербес реакциялары
Сулы ерітінділерде никель тұздары жасыл түсті береді.
І. Диметилглиоксим (Чугаев реактиві) аммиакты ортада никель катионымен Ni2+ ішкікомплекстік тұздың тұнбасын береді:
NiSO4 + 6NH4OH =  + 6H2O
+ 6H2O
 + 2C4H8N2O2 + 4H2O = Ni(C4H7N2O2)2↓ + (NH4)2SO4 + 4NH4OH
+ 2C4H8N2O2 + 4H2O = Ni(C4H7N2O2)2↓ + (NH4)2SO4 + 4NH4OH

NiSO4 + 2NH4OH + 2C4H8N2O2 = Ni(C4H7N2O2)2↓ + (NH4)2SO4 + 2H2O
1-тәжірибе. Пробиркаға никель тұзының 4 тамшысын құйып, оған сутектің асқын тотығының (Н2О2) 1-2 тамшысын және 5-6 тамшы концентрлі аммиак ерітіндісін қосыңдар, егер тұнба ерімесе оны сүзу қажет. Фильтраттың 1 тамшысын фарфор ыдысқа тамызып, оған диметилглиоксимнің 1 тамшысын қосыңдар. Егер никель катионы бар болса, онда ерітінді алдымен қарқынды ақшыл- қызыл түсті береді, сосын қызыл тұнба түзіледі.
Тәжірибені жүргізу шарттары:
1. Реакцияны рН=6-9 (аммиакты) ортада жүргізеді.
2. Егер темір (II) катионы бар болса, онда оны сутектің асқын тотығымен Fe3+ -ке дейін тотықтырыңдар.
3. Cu2+ мен Co2+ иондары никель Ni2+ иондарын анықтауға кедергі жасайды, сондықтан оларды бөліп тастау керек, себебі олар диметилглиоксиммен боялған қосылыс түзеді.
Не нашли, что искали? Воспользуйтесь поиском: