
ТОР 5 статей:
Методические подходы к анализу финансового состояния предприятия
Проблема периодизации русской литературы ХХ века. Краткая характеристика второй половины ХХ века
Характеристика шлифовальных кругов и ее маркировка
Служебные части речи. Предлог. Союз. Частицы
КАТЕГОРИИ:
- Археология
- Архитектура
- Астрономия
- Аудит
- Биология
- Ботаника
- Бухгалтерский учёт
- Войное дело
- Генетика
- География
- Геология
- Дизайн
- Искусство
- История
- Кино
- Кулинария
- Культура
- Литература
- Математика
- Медицина
- Металлургия
- Мифология
- Музыка
- Психология
- Религия
- Спорт
- Строительство
- Техника
- Транспорт
- Туризм
- Усадьба
- Физика
- Фотография
- Химия
- Экология
- Электричество
- Электроника
- Энергетика
Конечными продуктами обмена являются
1) ацетил-КоА
2) мочевина
3) пируват
4) вода
5) углекислый газ
3. Указать, в каких процессах не используется энергия, освобождающаяся при окислении питательных веществ
1) синтез АТФ
2) теплопродукция
3) осмотическая работа
4) гидролиз концевой фосфоангидридной связи АТФ
5) сокращение мышц
4. Центральную роль в энергообмене всех типов клеток осуществляет
1) креатинфосфат
2) электрохимический потенциал спрягающих мембран
3) ГТФ
4) система адениловых нуклеотидов
5. В молекуле АТФ макроэргической является связь
1) гликозидная
2) фосфоэфирная
3) фосфоангидридная
6. Указать, какое соединение не относится к макроэргическим
1) фосфоенолпируват
2) 1,3-дифосфоглицерат
3) глюкозо-6-фосфат
4) аденозинтрифосфат
5) цитидинфосфат
7. Реакция дегидрирования, в которой акцептором водорода служит не кислород, а химическое вещество, называется
1) тканевым дыханием
2) биологическим окислением
3) брожением
4) микросомальным окислением
8. Синтез АТФ в клетках эукариот протекает на
1) внутренней мембране митохондрий
2) наружной мембране митохондрий
3) мембранах ЭПР
4) плазматической мембране
9. Первичными акцепторами электронов от окисляемого субстрата к молекулярному кислороду являются
1) коэнзим Q
2) пиридинзависимые дегидрогеназы
3) цитохром b5
4) трансферрин
5) цитохром Р-450
10. Синтез АТФ за счет энергии, выделяющейся при переносе электронов от окисляемого субстрата к молекулярному кислороду, называют
1) субстратным фосфорилированием
2) окислительным фосфорилированием
3) фотофосфорилированием
Модуль № 4. «Обмен углеводов»
В организме человека и животных углеводы играют важную роль и выполняют разнообразные функции – служат источником энергии, являются пластическим материалом, используются в качестве исходных продуктов для синтеза липидов, белков и нуклеиновых кислот.
Организм человека и животных не способен синтезировать углеводы из неорганических веществ и получает их в готовом виде, главным образом с растительной пищей.
Суточная норма потребления углеводов – 400-500 г. Углеводы, поступившие в организм, подвергаются перевариванию в желудочно-кишечном тракте и всасываются в кровь в виде моносахаридов, в основном глюкозы.
Глюкоза, доставляемая кровью воротной вены в печень, превращается здесь в запасный углевод – гликоген, который откладывается в клетках печени. При необходимости гликоген печени расщепляется до глюкозы. Этой гликогенной функцией печени обеспечивается постоянное содержание сахара в крови. В крови всегда находится определенное количество глюкозы – 3,3-5,5 ммоль/л.
Содержание гликогена в печени не является постоянным и зависит прежде всего от состава пищи. В среднем содержание гликогена в печени человека около 6% веса органа, а общее количество гликогена в печени в среднем 100-120 г. Часть глюкозы откладывается в виде гликогена в других органах и тканях. Так как ассимиляционная способность печени имеет известный предел, то при введении большого количества углеводов с пищей часть резорбированного сахара проникает через печень в кровь, вызывая тем самым пищевую (алиментарную) гипергликемию. При некоторых заболеваниях, например, при диабете, содержание сахара в крови может возрастать в 2-3 раза по сравнению с нормой. Может наблюдаться и снижение содержания глюкозы ниже 3,3 ммоль/л. Так называемая гипогликемия, например, при тяжелых физических нагрузках (марафонский бег) приводит к обмороку. Установление гипо- и гипергликемии имеет большое диагностическое значение.
Поддержание определенной концентрации глюкозы в крови осуществляется благодаря сложным механизмам нейрогуморальной регуляции.
Лабораторная работа 1.
Определение глюкозы в крови (метод Хагедорна-Иенсена)
В основе определения глюкозы реакция восстановления феррицианида калия K3Fe(CN)6 в щелочной среде в присутствии глюкозы и других редуцирующих веществ (мочевой кислоты, креатинина, глутатиона и др.) в ферроцианид калия K4[Fe(CN)6], остаток невосстановленного K3[Fe(CN)6], определяют йодометрическим титрованием в кислой среде.
1.K3Fe(CN)6 + ГЛЮКОЗА = K4Fe(CN)6 + ОКИСЛЕННАЯ ГЛЮКОЗА +
K3Fe(CN)6(ОСТАТОК)
2. K3Fe(CN)6(ОСТАТОК) + 2KI = 2K4Fe(CN)6 + I2
3. I2 + 2Na2S2O3 = 2NaI + Na2S4O6
Материалы, реактивы, оборудование: 0,45% ZnSO4; 0,1N NaOH; 0,05 K3Fe(CN)6; 3% CH3COOH; 0,05Н щелочной раствор K3Fe(CN)6 (1,65 г K3Fe(CN)6 и 10,6 Na2CO3 безводный, в/л); тройной реактив а) 10 г ZnSO4 (без железа), 50 г NaСl в 200 мл Н2О, б) перед употреблением к 40 мл реактива А добавляют 1г KI, 0,005н Na2S2O3; 1% раствор крахмала; микробюретка, пробирки сахарные.
Ход работы:
1. В 4 пробирки наливают по 5 мл 0,45% раствора сульфата цинка и 1 мл 0,1 н гидроксида натрия. Образующийся гидроксид цинка используют для осаждения белов.
2. Две пробирки оставляют для контрольного опыта. В 2 другие вносят по 0,1 мл крови.
3. Все 4 пробирки помещают в кипящую водяную баню.
4. Содержимое пробирок отфильтровывают через воронки, заполненные ватой и дважды промывают водой по 2 мл. Промывные воды собирают.
5. К полученному фильтрату добавляют по 2 мл 0,005н K3Fe(CN)6.
6. Пробы вновь помещают в кипящую водяную баню на 15 минут.
7. Определяют остаток не прореагировавшей K3Fe(CN)6. Для этого добавляют по 2 мл 3% СН3СООН и 3 мл тройного реактива. Жидкость желтеет – выделяется свободный йод, который оттитровывают 0,005н раствором Na2S2O3 (гипосульфит) и 2 капли 1% раствора крахмала в качестве индикатора.
8. Содержание глюкозы определяют по таблице.
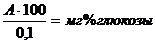 |
После проведения расчета определяют количество мг глюкозы в 100 мл крови, то есть мг/% глюкозы. Для этого по таблице определяют число в контрольной и опытной пробе и вычитают одно из другого. Полученную величину А переводят в мг/% по формуле.
Лабораторная работа 2.
Не нашли, что искали? Воспользуйтесь поиском: